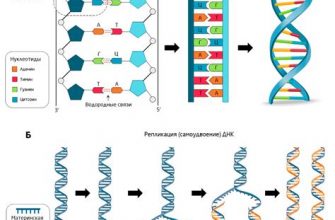
Процесс диссоциации солей и оснований является важным аспектом химических реакций, касающихся веществ, способных распадаться на ионы в растворе. Этот является ключевым процессом в химии и имеет большое значение для понимания реакций, происходящих между солями и щелочами.
Диссоциация представляет собой разделение молекул на ионы в растворе под воздействием растворителя, что позволяет образование электролитического раствора. Этот процесс часто происходит с солями, содержащими катионы металлов или аммония, и основаниями, включающими ионы гидроксилов.
Процесс диссоциации солей и оснований

Обычно диссоциация солей происходит полностью, а диссоциация оснований - частично. Например, NaCl полностью диссоциирует на ионы Na+ и Cl-, в то время как NaOH диссоциирует лишь на часть ионов Na+ и OH-.
Диссоциация солей и оснований играет важную роль в химических реакциях и в химических процессах, происходящих в живых организмах. Понимание этого процесса помогает в изучении химии и ее применении в различных областях.
Основные этапы диссоциации

Процесс диссоциации солей и оснований включает несколько ключевых этапов:
- Растворение в воде. Соль или основание распадаются на ионы при контакте с водой.
- Разделение на положительные ионы (катионы) и отрицательные ионы (анионы). Этот этап является основным для понимания диссоциации.
- Образование гидратированных ионов. Ионы, образовавшиеся после диссоциации, могут образовывать гидратированные комплексы с молекулами воды, что является важным шагом для понимания поведения растворов.
- Протекание химических реакций. После диссоциации ионы соли или основания могут участвовать в различных химических реакциях, что определяет их химические свойства и поведение в растворах.
Роль в химических реакциях
Процесс диссоциации солей и оснований играет важную роль в химических реакциях. При диссоциации молекулярных соединений солей и оснований их ионы реагируют с другими веществами, образуя новые соединения.
Ионы, выделенные при диссоциации, могут участвовать в различных химических процессах, например, в реакциях окисления-восстановления, образовании осадков или обмене ионами.
Таким образом, диссоциация солей и оснований не только является ключевым этапом в химических реакциях, но и определяет химические свойства и возможные реакции данных веществ.
Соли как электролиты

Соли, в растворе или расплавленном виде, также способны диссоциировать на ионы, что делает их электролитами. Диссоциация солей происходит на ионы металла и анионы, которые образуют соль. Примером может служить раствор кухонной соли (хлорида натрия), который диссоциирует на натриевые и хлоридные ионы.
Ионы, образующиеся при диссоциации солей, обуславливают проводимость растворов солей.
Так, растворы солей являются хорошими проводниками электричества, поскольку ионы, образующиеся при диссоциации, могут перемещаться в растворе и обеспечивать проводимость. Это свойство солей широко используется в различных областях химии и технологий.
Основания и их свойства

Свойства оснований:
- Основания обладают щелочным вкусом и способностью изменять цвет индикаторов;
- Определяют степень основания по Лавруа величиной щелочности;
- Основания растворяются в воде, образуя гидроксиды металлов.
Взаимодействие оснований с кислотами

Взаимодействие оснований с кислотами играет ключевую роль в процессе нейтрализации, когда кислота и основание нейтрализуют друг друга, образуя соль и воду.
Примеры реакций диссоциации

Реакция диссоциации солей может происходить следующим образом:
NaCl → Na+ + Cl-
В данном случае хлорид натрия (NaCl) расщепляется на положительный ион натрия (Na+) и отрицательный ион хлора (Cl-).
Основание, такое как гидроксид натрия, также может диссоциировать:
NaOH → Na+ + OH-
Гидроксид натрия (NaOH) расщепляется на ионы натрия (Na+) и гидроксидные ионы (OH-).
Вопрос-ответ

Что такое процесс диссоциации солей в химии?
Процесс диссоциации соли в химии представляет собой распад молекулы соли на ионы в растворе. Этот процесс происходит при контакте с водой, где положительные ионы катионов переходят в раствор, образуя положительный заряженный ион, а отрицательные ионы анионов также переходят в раствор, образуя отрицательный заряженный ион. Процесс диссоциации солей играет важную роль в химии, особенно при реакциях в растворах.
Как происходит диссоциация оснований в химии?
Диссоциация оснований в химии аналогична диссоциации солей. При контакте с водой основание распадается на ионы, формируя положительные ионы катионов и отрицательные ионы анионов. Ионы образуются из молекул основания при контакте с раствором. Диссоциация оснований является важным процессом в химии и используется в различных химических реакциях и процессах.
Какие основные моменты следует запомнить о процессе диссоциации солей и оснований в химии?
Основные моменты процесса диссоциации солей и оснований в химии включают в себя понятие распада молекул на ионы при контакте с раствором, образование положительных и отрицательных ионов, значимость данного процесса для понимания реакций в растворах, а также применение диссоциации солей и оснований в различных химических процессах и реакциях.
Почему процесс диссоциации солей и оснований важен в химии?
Процесс диссоциации солей и оснований важен в химии, так как позволяет понять, как происходит распад молекул на ионы в растворе, что является основой для понимания химических реакций, проводимых в растворах. Диссоциация солей и оснований используется в различных химических процессах, что делает данный процесс одним из ключевых в химии.