Малый период в химии – это важное понятие, которое помогает упорядочить элементы в периодической системе химических элементов. Он представляет собой группу химических элементов, у которых по порядку изменяется число зарядов ядра. Малый период включает элементы одной группы химических элементов с одинаковым числом внешних электронов в оболочке.
Для понимания химических свойств элементов и установления закономерностей в их поведении важно изучать ключевые аспекты малого периода. К ним относятся электронная конфигурация, химические свойства и активность элементов, а также их положение в периодической системе.
Особенности малого периода в химии заключаются в том, что элементы в нем имеют сходные химические свойства и могут образовывать аналогичные соединения. Это позволяет установить связи между элементами и предсказывать их поведение в различных химических реакциях.
Роль малого периода

Малый период в химии играет ключевую роль в систематизации элементов и предсказании их свойств. Он включает элементы схожих химических свойств и структурой электронных оболочек, что позволяет лучше понять химическое поведение этих элементов. Кроме того, изучение элементов малого периода помогает установить закономерности в периодической системе Менделеева и прогнозировать химические реакции и свойства новых элементов.
Понимание роли малого периода не только важно для химиков, но и является основой для дальнейших исследований и разработок в области химии и материаловедения.
Важность химического разделения

Кроме того, химическое разделение позволяет нам выполнять анализ химических составов смесей, определять их структуру и устанавливать концентрацию различных компонентов. Это необходимо для контроля качества продукции, исследования окружающей среды, а также для проведения медицинских и научных исследований.
Обществу необходимы специалисты, которые владеют методами химического разделения и могут успешно применять их в различных областях науки и промышленности. Поэтому изучение и понимание принципов химического разделения является важным звеном в образовании будущих специалистов и развитии научных и технических отраслей.
Открытие элементов

Каждое открытие нового элемента приводило к расширению наших знаний о мире химии и позволяло ученым лучше понять строение вещества. Эти открытия являются важными шагами в развитии науки и имеют большое значение для практического применения в различных областях жизни.
- Первыми элементами, открытыми в малый период химии, были металлы, такие как железо, медь, олово и другие, которые играли важную роль в различных процессах и технологиях.
- Со временем были открыты и другие элементы, включая редкоземельные металлы, инертные газы, радиоактивные элементы и многое другое.
- Открытие новых элементов продолжается и сегодня, и каждое новое открытие открывает перед учеными новые возможности для исследования и применения в различных областях науки и техники.
Основные элементы
Малый период в химии включает элементы, атомы которых имеют одинаковое количество корневых электронов во внешнем энергетическом уровне. К ним относятся элементы групп 1 (щелочные металлы) и группы 2 (щелочноземельные металлы). Основные характеристики этих элементов связаны с их химическими свойствами и реактивностью, которая определяется степенью вовлеченности внешних электронов в химические реакции.
Химические свойства

Малый период в химии характеризуется особыми химическими свойствами элементов, находящихся в его составе. Эти элементы обладают сходными химическими реакциями и формируют типичные соединения, которые могут обнаруживаться в природе или быть синтезированными в лаборатории. Важно отметить, что малый период, включающий элементы от лития до неона, имеет специфические химические свойства и требует отдельного изучения.
Например, элементы первой группы (литий, натрий, калий и др.) обладают химическими свойствами металлов: они активно реагируют с водой, образуя гидроксиды и выделяя водород. Элементы второй группы (бериллий, магний, кальций и др.) также имеют сходные химические свойства, образуя оксиды и гидроксиды.
Таким образом, изучение химических свойств элементов малого периода позволяет понять их поведение в химических реакциях и определить возможные способы взаимодействия с другими веществами.
Физические свойства
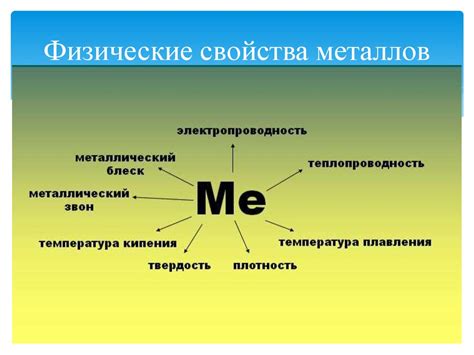
Малый период химического элемента определяет его физические свойства, такие как плотность, температура плавления, температура кипения, твердость и прочие физические характеристики. Эти свойства зависят от структуры внешних электронных оболочек атомов элемента, а также от его массы и заряда ядра.
Особенности физических свойств элементов в малом периоде отражаются в пространственной структуре их кристаллической решетки, которая влияет на их механическую прочность, способность к излучению и поглощению энергии, а также на их теплопроводность и электропроводность.
| Свойство | Описание |
|---|---|
| Плотность | Отражает массу элемента на единицу объема и зависит от массы атомов и структуры кристаллической решетки. |
| Температура плавления | Температура, при которой элемент переходит из твердого состояния в жидкое. |
| Температура кипения | Температура, при которой жидкость переходит в газообразное состояние. |
| Твердость | Свойство материала сопротивляться деформации и истиранию при нагрузке. |
Природное распространение
Современная химия получила важные указания от малой химии в отношении природного распространения элементов и их соединений. Многие элементы были обнаружены и идентифицированы в природе благодаря изучению минералов, руд и органических материалов. Например, железо может быть найдено в различных минералах, таких как гематит и магнетит. Открытие и исследование природных источников элементов играет важную роль в развитии и понимании химии как науки.
Нахождение в природе

| Элемент | Области нахождения в природе |
|---|---|
| Гелий (He) | Главным образом в атмосфере, в газовых месторождениях |
| Литий (Li) | Различные минералы, моря и водные источники |
| Бериллий (Be) | Минералы берилла, рудные месторождения |
| Углерод (C) | Широко распространен в органических соединениях, в виде алмазов и графита |
| Азот (N) | Основной компонент атмосферы, в виде различных соединений в почве и организмах |
| Кислород (O) | Широко распространен в атмосфере, в воде, минералах и органических соединениях |
| Бор (B) | Минералы бора и его соединения, гидротермальные источники |
Вопрос-ответ

Чем определяется малый период в химии?
Малый период в химии определяется периодическим законом, согласно которому свойства химических элементов изменяются периодически с увеличением порядкового номера элемента в таблице Менделеева. Малый период состоит из элементов, которые находятся в одном периоде таблицы Менделеева.
Какие особенности характеризуют малый период в химии?
Основные особенности малого периода в химии включают в себя сходство химических свойств элементов данного периода, изменение электронной конфигурации элементов и их атомных радиусов вдоль периода, а также периодическое увеличение электроотрицательности элементов.
Какие ключевые аспекты важны для понимания малого периода в химии?
Для понимания малого периода в химии необходимо учитывать строение атомного ядра и оболочек атомов, взаимодействие электронов на разных энергетических уровнях, связанных с изменением порядкового номера химических элементов в периоде, а также химические свойства и тенденции изменения в периодической системе.
Почему малый период считается важным в химии?
Малый период играет важную роль в химии, поскольку позволяет установить закономерности в изменении химических свойств элементов в таблице Менделеева, что помогает предсказывать и объяснять реакции и соединения веществ. Понимание малого периода позволяет углубить знания о строении атомов и их взаимодействии.