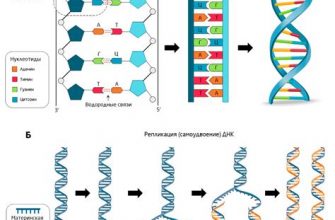
Глобулярные белки - это класс белков, которые имеют шарообразную структуру и обладают высокой растворимостью в воде. Они играют важную роль в организме, участвуя в широком спектре биологических процессов.
Основной причиной растворимости глобулярных белков в воде является их уникальная структура, которая обеспечивает специфические взаимодействия с молекулами воды. Благодаря гидрофильным аминокислотным остаткам, глобулярные белки способны образовывать водородные связи и взаимодействовать с полярными группами воды.
Также важную роль играют гидрирующие свойства воды, которые позволяют эффективно сдерживать электрические заряды на поверхности белков, способствуя их стабилизации и растворимости. Все эти факторы совместно обуславливают способность глобулярных белков быть растворимыми в воде.
Глобулярные белки: растворимость в воде
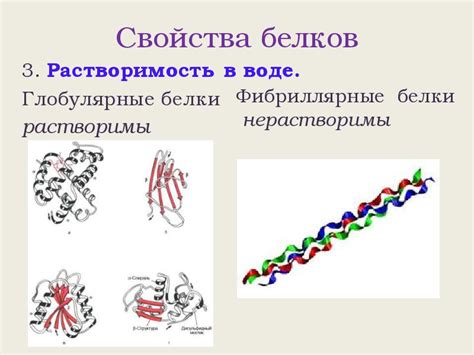
| 1. Структура | Глобулярные белки имеют компактную шарообразную структуру, которая способствует хорошему взаимодействию с водой. |
| 2. Гидрофильность | Белки содержат аминокислотные остатки, способные образовывать водородные связи и взаимодействовать с полярными молекулами воды. |
| 3. Гидрофобные области | Хотя глобулярные белки содержат гидрофобные области, они укрывают их в своей структуре, как бы "скрывая" от воды, что также способствует растворимости. |
Эти факторы в сочетании делают глобулярные белки отлично растворимыми в воде и играют значительную роль в их функционировании в организмах живых существ.
Природа глобулярных белков
| Амфифильность | Глобулярные белки содержат гидрофильные остатки аминокислот на поверхности молекулы, и гидрофобные остатки - внутри. Эта амфифильность способствует растворению белков в воде, так как гидрофильные остатки взаимодействуют с молекулами воды, а гидрофобные остатки скрыты внутри молекулы. |
| Гидрофильность | Глобулярные белки содержат обильное количество поларных и заряженных аминокислот, которые способствуют образованию водородных связей, ионных взаимодействий и дисперсионных сил между белками и молекулами воды, обеспечивая их растворимость в воде. |
Таким образом, амфифильность и гидрофильность глобулярных белков являются основными причинами их высокой растворимости в воде, что является важным для их функционирования в организме.
Химические свойства структуры

Глобулярные белки отличаются от строения других белков своей компактной трехмерной формой. Их структура обычно содержит много спиральных и петлевидных участков, что обеспечивает им высокую растворимость в воде. Гидрофильные аминокислоты, находящиеся на поверхности глобул, взаимодействуют с молекулами воды, образуя водородные связи и электростатические взаимодействия. Это делает их растворимыми и стабильными в водной среде.
Компактная структура глобуларных белков также способствует их способности сворачиваться в шарообразные формы при изменении условий окружающей среды, например, при изменении pH или температуры. Это позволяет им легко выполнять свои функции и быть вовлеченными в разнообразные биологические процессы в организме.
Взаимодействие с водой

Глобулярные белки хорошо растворимы в воде из-за их структуры. Они содержат большое количество полюсных аминокислот, таких как серин, треонин и аспартат, которые способствуют образованию водородных связей с молекулами воды.
Под влиянием водородных связей между аминокислотами и водой глобулярные белки образуют гидратированные оболочки, что способствует их растворению в воде. Кроме того, гидрофильные аминокислоты, содержащиеся в глобулярных белках, взаимодействуют с молекулами воды, обеспечивая устойчивость раствора.
Этот механизм взаимодействия с водой делает глобулярные белки важными компонентами в клеточных процессах и обеспечивает их функциональность в организме.
Электростатические силы притяжения

Электрические взаимодействия между заряженными группами аминокислот в белковой молекуле и диполями водных молекул обеспечивают эффективное взаимодействие и удерживание глобулярной структуры белка в растворе.
Формирование водородных связей
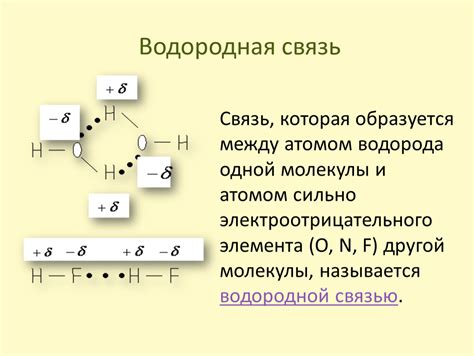
Водородные связи обычно образуются между положительно заряженным водородом и отрицательно заряженным кислородом, нитрогеном или другим атомом. Эти слабые связи обеспечивают устойчивость структуры белка, позволяя ему оставаться в растворенном состоянии в воде.
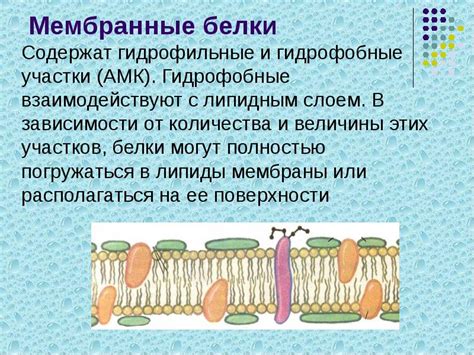
Гидрофобные участки структуры
Специфичность действия воды
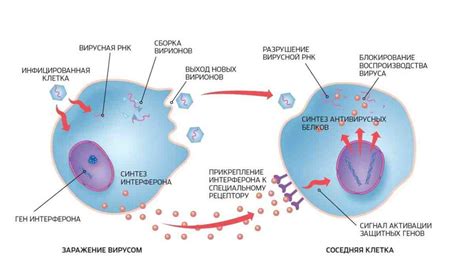
Глобулярные белки имеют специфическую структуру, которая обеспечивает их растворимость в воде. Эта специфичность заключается в том, что глобулярные белки содержат большое количество положительно и отрицательно заряженных аминокислотных остатков. Эти заряженные группы привлекают молекулы воды, образуя водородные связи и ионо-дипольные взаимодействия, что способствует стабилизации белка в воде.
Этот механизм взаимодействия помогает глобулярным белкам сохранять свою стабильность и функциональную активность при контакте с водой, делая их необходимыми для многих биологических процессов в организме.
Универсальность растворения

Глобулярные белки обладают уникальной способностью растворяться в воде благодаря своей структуре и функциональным группам. Это позволяет им быть универсальными катализаторами химических реакций в клетках организма, участвовать в транспорте различных веществ и обеспечивать поддержание гомеостаза. Благодаря возможности растворяться в воде глобулярные белки могут быть эффективно использованы в медицине, пищевой промышленности и других областях, где требуется высокая растворимость в воде.
Значение для биологических процессов

Глобулярные белки играют важную роль в биологических процессах, так как они способны растворяться в воде и образовывать стойкие дисперсные системы. Это позволяет им участвовать в транспорте различных молекул и ионов через клеточные мембраны, а также в регуляции метаболических процессов в организме.
Благодаря своей способности к растворению, глобулярные белки могут выполнять функции переноса кислорода, связывания гормонов, антибиотиков и других биологически активных веществ, а также участвовать в иммунных реакциях и коагуляции крови.
Факторы, влияющие на растворимость

Растворимость глобулярных белков в воде определяется рядом факторов, включая:
- Структура белка: Глобулярные белки имеют компактную структуру, что способствует их растворимости в воде. Это связано с высоким содержанием поларных аминокислот, способных образовывать водородные связи с молекулами воды.
- Гидратация: Гидратация белковых молекул водой способствует их растворению за счет образования водородных связей между поларными группами белка и водой.
- pH среды: Растворимость глобулярных белков может зависеть от pH среды из-за изменения заряда аминокислотных остатков в структуре белка. Оптимальное pH для растворения различных белков может быть разным.
- Температура: Температура также оказывает влияние на растворимость белков. Увеличение температуры может способствовать разрушению водородных связей и изменению конформации белка, что повлияет на его растворимость.
Изучение этих факторов позволяет понять механизмы растворения глобулярных белков в воде и их поведение в различных условиях.
Вопрос-ответ

Почему глобулярные белки растворимы в воде?
Глобулярные белки растворимы в воде благодаря своей трехмерной структуре, которая создает гидрофильные поверхности, способные взаимодействовать с молекулами воды. Это происходит за счет присутствия в их структуре множества поларных аминокислотных остатков, способных образовывать водородные связи с водой.
Какие основные причины делают глобулярные белки растворимыми в воде?
Основной причиной, по которой глобулярные белки растворимы в воде, является гидратация и гидрофильность их поверхности. Гидратация происходит из-за того, что поверхность белка обладает множеством поларных аминокислот, которые могут образовывать водородные связи с молекулами воды, обеспечивая их растворение.
Как глобулярные белки взаимодействуют с водой?
Глобулярные белки взаимодействуют с водой благодаря своей трехмерной структуре, которая обладает гидрофильными участками, способными привлекать молекулы воды. Эти белки могут образовывать водородные связи и иные взаимодействия с молекулами воды, что обеспечивает их растворение в воде.
В чем заключается особенность гидратации глобулярных белков в воде?
Особенность гидратации глобулярных белков в воде заключается в их способности привлекать молекулы воды к поверхности в результате образования водородных связей и других взаимодействий. Это обеспечивает их растворимость, так как поверхность белков остается окруженной слоем водных молекул, обеспечивая стабильность и функционирование белков в водной среде.