Сера – это химический элемент, который обладает множеством интересных свойств и находит широкое применение в различных отраслях промышленности. Одна из важных характеристик серы заключается в ее способности вступать в реакции с различными металлами. При этом, химические свойства серы могут существенно отличаться в зависимости от металла, с которым она взаимодействует.
Одним из примеров таких реакций является реакция серы с железом. При нагревании серы и железа в атмосфере кислорода происходит образование соединения FeS. Данная реакция является примером реакции окисления-восстановления, в которой два вещества обмениваются электронами. При этом, сера окисляется, а железо восстанавливается.
Кроме того, сера может образовывать соединения и с другими металлами, например, с медью. Реакция меди с серой в результате термического воздействия приводит к образованию соединения CuS. Это весьма стабильное соединение, которое применяется в различных отраслях промышленности, включая производство полупроводников и пигментов.
Таким образом, реакции серы с различными металлами представляют особый интерес в химии и имеют важное практическое значение. Они могут приводить к образованию различных соединений, которые обладают разными свойствами и находят применение в разных областях науки и промышленности.
Взаимодействие серы с металлами: особенности и свойства

Одним из наиболее известных примеров взаимодействия серы с металлами является образование сернистого ацида. При этом происходит реакция сульфидирования металла, в результате которой белый порошок серы проникает в поверхностный слой металла, образуя стабильное соединение.
Сера может также образовывать сульфаты металлов – соединения, в которых сера связана с металлическими ионами. Эти соединения обладают различными свойствами в зависимости от металла, с которым сера образует соединение.
Взаимодействие серы с металлами может также приводить к образованию пятен, коррозии и разрушению металлических поверхностей. Сера может представлять собой агрессивное окружающее вещество, способное разрушать металлы, особенно влажные.
Важно отметить, что взаимодействие серы с металлами имеет как положительные, так и отрицательные стороны. С одной стороны, это позволяет использовать серные соединения в различных областях промышленности и науки. С другой стороны, необходимо учитывать возможность коррозии и разрушения металлических конструкций, вызванных взаимодействием с серой.
Металлы, c которыми образуются соединения

Сера образует соединения с различными металлами, что придает им разнообразные свойства и применения. Некоторые из наиболее распространенных металлов, с которыми образуются соединения серы, включают:
- Железо: сера может образовывать с железом различные соединения, включая сульфиды, сульфаты и серосодержащие органические соединения. Например, сульфид железа широко используется в промышленности для производства стали и других металлических сплавов.
- Медь: медь и сера могут образовывать различные соединения, такие как сульфид меди, который имеет ярко-черный цвет и широко используется в ювелирном искусстве и в производстве электроники.
- Свинец: сера и свинец могут образовывать соединения, такие как сульфид свинца, который широко используется в производстве аккумуляторов и других электронных устройств.
- Цинк: сера может реагировать с цинком, образуя сульфид цинка, который используется в промышленности для производства резиновых изделий и жестяной упаковки.
- Алюминий: сера и алюминий могут образовывать различные соединения, такие как алюминий сульфат, который широко используется в качестве вяжущего в строительной отрасли.
Это лишь некоторые из металлов, с которыми образуется соединения серы. Комбинирование серы с различными металлами позволяет создавать разнообразные материалы с различными свойствами и применениями.
Физические свойства получаемых соединений

Соединения, образующиеся при реакциях серы с металлами, обладают различными физическими свойствами, которые могут быть полезными в различных областях науки и промышленности:
- Вещества, полученные в результате реакции серы с некоторыми металлами, обладают хорошей твердостью и прочностью. Это делает их полезными для использования в производстве материалов с повышенной износостойкостью, таких как стальные сплавы.
- Некоторые соединения серы и металлов имеют высокую плотность, что делает их ценными материалами для использования в аэрокосмической и авиационной промышленности.
- Некоторые соединения серы и металлов обладают специфическими магнитными свойствами, такими как ферромагнетизм. Это позволяет использовать их в производстве магнитов и других устройств, связанных с магнитным полем.
- Некоторые соединения серы и металлов имеют высокую точку плавления и кипения, что делает их полезными в производстве материалов с высокой стабильностью и термической устойчивостью.
- Некоторые соединения серы и металлов обладают хорошей проводимостью электрического тока. Это делает их полезными для использования в электронике и электротехнике.
Таким образом, соединения, получаемые при реакциях серы с различными металлами, представляют собой разнообразные материалы с уникальными физическими свойствами, что открывает широкие возможности их применения в различных областях науки и промышленности.
Химические свойства образованных веществ

В результате реакции серы с различными металлами образуются соединения, которые обладают различными химическими свойствами.
Например, при реакции серы с железом образуется железная сера, которая обладает темно-серым цветом и не растворяется в воде. Ее основное свойство – это высокая степень стабильности, благодаря которой она может длительное время сохраняться без изменений.
Реакция серы с медью приводит к образованию медной серы, имеющей красно-коричневый цвет. Она обладает высокой растворимостью в воде и хорошо проводит электрический ток. Медная сера также является окислителем и может взаимодействовать с другими веществами.
Реакция серы с алюминием приводит к образованию серы алюминия, которая имеет белый цвет и плохо растворяется в воде. Это вещество обладает высокой теплостойкостью и может использоваться в промышленности в качестве реагента.
Таким образом, образовавшиеся вещества при реакции серы с различными металлами обладают различными химическими свойствами, что делает их полезными в различных областях науки и промышленности.
Реакция серы с щелочными металлами

Щелочные металлы, такие как натрий и калий, обладают свойством активно реагировать с серой. Это связано с их высокими степенями восстановления и электроотрицательностью.
Реакция между щелочными металлами и серой протекает при нагревании и сопровождается выделением высокой энергии. В результате образуются сульфиды щелочных металлов.
Примером реакции может служить реакция натрия с серой:
| Реакция: | Уравнение: | Продукты: |
|---|---|---|
| Натрий + сера | 2Na + S → Na2S | Сульфид натрия |
Сульфид натрия имеет характерную желтую окраску и обладает специфическим запахом. Он является твердым веществом и растворим в воде.
Реакция серы с другими щелочными металлами, такими как калий и литий, протекает аналогичным образом. Образующиеся сульфиды щелочных металлов также имеют яркую окраску.
Реакция серы с щелочными металлами является важным аспектом в химии и находит применение в множестве технологических процессов и синтезе различных соединений.
Реакция серы с щелочноземельными металлами

Щелочноземельные металлы, такие как магний, кальций и барий, проявляют характерные особенности при взаимодействии с серой. Реакции этих металлов с серой могут происходить при нагревании или при действии кислорода.
Когда щелочноземельные металлы нагреваются с серой, происходит образование соответствующих серосоединений. Например, магний может образовывать серурид магния (MgS), кальций - серурид кальция (CaS), а барий - серурид бария (BaS). Эти соединения обычно имеют белый цвет.
Реакции щелочноземельных металлов с серой также могут протекать при наличии кислорода. В этом случае образуются сульфаты металлов. Например, при сжигании магния в воздухе формируется оксид магния, который взаимодействует с серой, образуя сульфат магния (MgSO4). Кальций и барий также могут образовывать аналогичные соединения - сульфаты кальция (CaSO4) и бария (BaSO4).
Реакция серы с щелочноземельными металлами может быть сопровождена выделением газов. Например, при нагревании серы с магнием образуется сернистый газ (SO2), который активно используется в различных отраслях промышленности.
Химические свойства щелочноземельных металлов определяются их электрохимическими характеристиками. Они имеют высокую реакционную способность, что позволяет им образовывать стабильные соединения с серой.
Реакция серы с щелочноземельными металлами является важным аспектом изучения химии данных элементов. Она позволяет понять их химические свойства и применение в различных областях науки и техники.
Взаимодействие серы со среднетяжелыми металлами
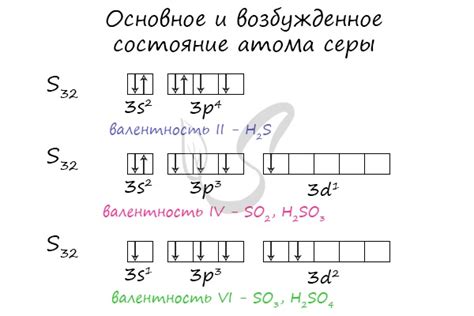
Одной из важнейших характеристик серы является ее способность окислять металлы. При контакте с серой металлы могут подвергаться окислению, что приводит к образованию соответствующих оксидов. Например, при взаимодействии серы с медью образуется серный диоксид (SO2) и оксид меди (CuO). Эта реакция может быть представлена следующим уравнением:
S + Cu → SO2 + CuO
Кроме окисления металлов, сера способна взаимодействовать с ними и образовывать сложные соединения. Например, сера может реагировать с железом и образовывать серное железо (FeS) или с марганцем, образуя марганцевый сульфид (MnS). Эти реакции могут быть представлены следующими уравнениями:
S + 2Fe → FeS
S + Mn → MnS
Кроме того, сера может взаимодействовать со среднетяжелыми металлами и образовывать различные соли серы. Например, при реакции серы с цинком может образоваться сернокислый цинк (ZnSO4). Уравнение этой реакции имеет следующий вид:
S + Zn → ZnSO4
Таким образом, взаимодействие серы со среднетяжелыми металлами является сложным и может сопровождаться разнообразными химическими реакциями. Изучение этих реакций позволяет лучше понять свойства серы и ее влияние на металлы.
Реакция серы с переходными металлами

Одной из наиболее распространенных реакций серы с переходными металлами является образование сульфидов. Сера может реагировать с металлами, образуя различные типы сульфидов: металлические сульфиды, полисульфиды и соединения с ионами серы в различных степенях окисления.
Образование металлических сульфидов происходит путем прямой реакции серы с металлом. Например, реакция серы со железом приводит к образованию ферросульфида:
- Fe + S → FeS
Особенностью реакций серы с переходными металлами является возможность образования различных типов сульфидов в зависимости от условий реакции. Например, сульфид железа может образовываться в разных формах: моносульфид (FeS), дизульфид (FeS2) и др.
Кроме того, сера может реагировать с переходными металлами, образуя различные полисульфиды. Полисульфиды представляют собой соединения, в которых в молекуле присутствуют несколько атомов серы, связанных между собой. Образование полисульфидов может происходить путем прямой реакции серы с металлом или путем окисления сульфидов переходного металла.
Реакции серы с переходными металлами также могут приводить к образованию соединений с ионами серы в различных степенях окисления. Например, сера может окисляться до иона серы VI и образовывать сульфаты переходного металла, такие как сульфат меди(II):
- 2Cu + S8 + 8H2O → 2CuSO4 + 8H2S
Реакции серы с переходными металлами имеют широкое промышленное применение. Например, сульфиды переходных металлов используются в качестве катализаторов, пигментов, полупроводников и других материалов. Кроме того, соединения серы с переходными металлами могут быть использованы в процессах обогащения полезных ископаемых и в других технологических процессах.
Применение серосодержащих соединений

Серосодержащие соединения широко применяются в различных областях нашей жизни благодаря их уникальным химическим свойствам. Вот некоторые примеры использования серосодержащих соединений:
1. Производство удобрений: Серосодержащие соединения, такие как сера и сульфаты, используются в производстве удобрений. Они обеспечивают растениями необходимый серный элемент, который является важным для их нормального роста и развития.
2. Горное дело: Серосодержащие соединения, например сернистый ангидрид, применяются в горной промышленности для обработки рудных материалов. Они помогают извлечь ценные металлы, такие как золото и медь, из руды.
3. Производство резин: Серосодержащие соединения используются в процессе вулканизации резиновых изделий. Это позволяет добиться повышенной прочности и устойчивости к износу резины.
4. Производство красителей: Серосодержащие соединения являются важными компонентами в производстве различных красителей. Они придают краске яркость и интенсивность цвета.
5. Производство фармацевтических препаратов: Некоторые серосодержащие соединения используются в производстве фармацевтических препаратов. Они могут иметь противовоспалительное, антибактериальное или антигрибковое действие.
Это всего лишь несколько примеров применения серосодержащих соединений. Благодаря своим уникальным химическим свойствам, эти соединения находят применение во многих других отраслях, включая пищевую промышленность, производство бумаги, текстиля и многих других.