Второй закон термодинамики является одним из фундаментальных принципов физики, описывающим направление тепловых процессов в природе. Он формулирует, что теплота сама от себя не переходит из холодного тела в горячее и требует для этого затраты энергии. Этот закон важен для понимания многих явлений, происходящих в природе и технике.
Основной идеей второго закона термодинамики является понятие энтропии – меры беспорядка системы. Закон утверждает, что в изолированной системе энтропия всегда возрастает или остается постоянной. Это означает, что процессы, происходящие в природе, направлены к увеличению беспорядка системы и разрушению упорядоченной структуры вещества.
Роль второго закона

Роль второго закона термодинамики заключается в определении того, как система эволюционирует со временем. Этот закон позволяет предсказать, какие процессы будут происходить в системе и как изменится ее состояние.
| Примеры: | 1. Нагревание чашки кофе: тепло из горячего кофе передается в окружающую среду, пока температуры не выровняются. |
|---|---|
| 2. Распад радиоактивного вещества: радиоактивные атомы естественным образом распадаются, увеличивая энтропию системы. |
Объяснение термодинамики
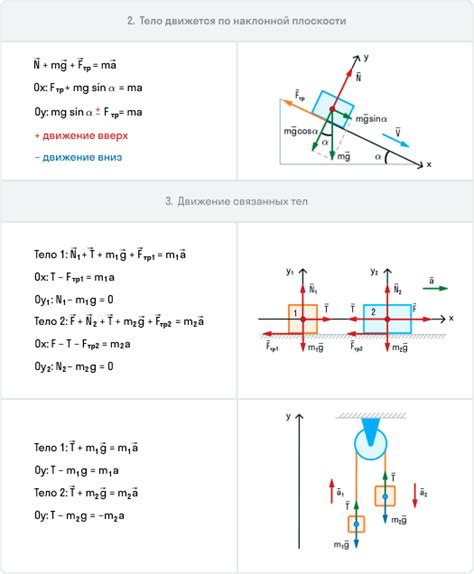
Этот закон можно объяснить на примере процесса, например, когда горячее тело контактирует с холодным телом, теплота передается от горячего к холодному. В результате уровень энтропии системы увеличивается, что приводит к равновесию температур и изменению состояния системы.
Таким образом, Второй закон термодинамики отражает необратимость процессов в природе и имеет важное значение для понимания энергетических потоков и изменений в системах.
Принцип энтропии

Принцип энтропии объясняет, почему песчинки разлетаются по столу, но не собираются обратно в песчинку. Это связано с тем, что система стремится к увеличению своей энтропии, и возврат к более упорядоченному состоянию (например, песчинке) требует большего энергетического затрат и не является естественным процессом.
Изменение состояний системы
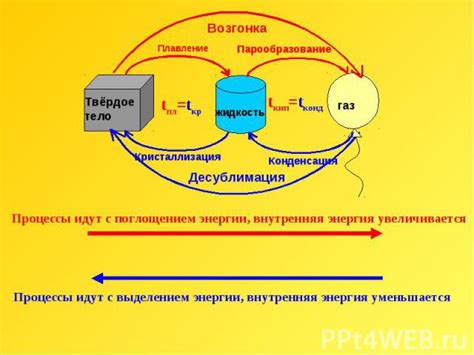
Система может находиться в различных состояниях в зависимости от ее энергетического уровня. При взаимодействии с окружающей средой система может изменять свое состояние и терять или приобретать энергию. Изменение состояний системы происходит в соответствии со вторым законом термодинамики, который утверждает, что энтропия системы всегда стремится к увеличению.
Процессы изменения состояний системы могут быть различными, включая адиабатические, изотермические, изохорические, и изобарические процессы. В каждом случае система переходит из одного состояния в другое, сопровождаясь изменением ее внутренней энергии и энтропии.
| Тип процесса | Характер изменения состояния |
|---|---|
| Адиабатический | Без теплообмена с окружающей средой |
| Изотермический | При постоянной температуре системы |
| Изохорический | При постоянном объеме системы |
| Изобарический | При постоянном давлении системы |
Понятие теплового равновесия
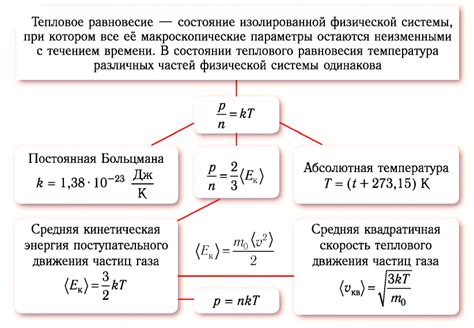
Система достигает теплового равновесия, когда все части системы имеют одинаковую температуру и тепло не переходит между ними без внешнего воздействия. Тепловое равновесие также означает, что все процессы, связанные с теплопередачей, прекращаются, и система остается в этом состоянии до воздействия внешних факторов.
Вопрос-ответ

Что такое второй закон термодинамики и как он объясняется?
Второй закон термодинамики утверждает, что тепло не может самопроизвольно перетекать от объекта с более низкой температурой к объекту с более высокой температурой. Это можно объяснить через понятие энтропии – меры беспорядка системы. Согласно второму закону, энтропия изолированной системы всегда увеличивается или остается постоянной.
Какой пример можно привести для наглядного объяснения второго закона термодинамики?
Один из классических примеров, иллюстрирующих второй закон термодинамики – это процесс теплопроводности. Когда горячий объект находится рядом с холодным объектом, тепло будет перетекать от горячего к холодному, но никогда наоборот, то есть из холодного объекта к горячему, в соответствии с вторым законом.
Как второй закон термодинамики связан с концепцией энтропии?
Второй закон термодинамики тесно связан с концепцией энтропии. Энтропия – это мера беспорядка системы. Согласно второму закону, энтропия изолированной системы всегда увеличивается или остается постоянной. Это означает, что система стремится к состоянию с наибольшей энтропией, к тому, что мы воспринимаем как более хаотичное состояние.